Cette petite étude présente le principe théorique d'une datation, le déroulement d'une expérience de datation, les différentes applications d'une datation, et l'analyse des limites de la méthode. Elle est suivie d'un exposé sur la datation du Suaire de Turin et d'autres reliques.
Dans le cadre des recherches historiques et scientifiques du Shroud Science Group sur le Suaire de Turin, nous présentons dans cette étude les méthodes utilisées par le laboratoire du C.D.R.C. pour la datation par radioactivité, et plus particulièrement par le Carbone 14.
Plus qu'un simple article, nous avons essayé de réaliser une étude approfondie sur ce sujet en nous basant sur les documents fournis par ce laboratoire, afin de fournir une base de discussion précise aux membres du Shroud Science Group.
PRINCIPE D'UNE DATATION
Pourquoi le Carbone 14 ?
Depuis plusieurs siècles déjà, les scientifiques dataient les objets archéologiques selon les strates dans lesquelles ils étaient découverts (stratigraphie). Ils comparaient les différents lits de strates et pouvait ainsi les dater, les strates inférieures étant considérées comme plus anciennes que les strates supérieures. Grâce à cette technique les chercheurs ont divisé l'histoire de la Terre en 4 grandes parties: Précambrien, Paléozoïque, Mésozoïque et Cénozoïque.
A la fin du 19ème siècle, lors de la découverte de la radioactivité par les français Henri Becquerel et le couple Pierre et Marie Curie, la possibilité d'utiliser les éléments radioactifs pour les datations commença à être envisagée. L'isotope du carbone fut ensuite découvert presque fortuitement en 1934 lorsqu'un physicien Américain, F.N.F. Kurie, exposa de l'azote à un flux de neutrons.
Mais la véritable découverte du radiocarbone naturel, date de 1946, lorsque Willard Franck Libby, un chimiste américain, émit l'idée d'une production continue de cet isotope dans la nature et établit les bases théoriques et pratiques de son utilisation en vue de datations en Archéologie.
Libby montra que le tritium, isotope de l'hydrogène, est produit par les radiations cosmiques. En 1947, il mit au point, avec ses étudiants, la technique de datation au carbone 14. Il eut l'idée d'étudier la proportion de carbone 14 dans deux objets en bois provenant d'une tombe égyptienne, et réalisa ainsi la première datation par radioactivité de l'Histoire, ce qui lui vaudra un Prix Nobel de Chimie en 1960.
Les premiers résultats de W.F. Libby en 1949 et 1950 et la mise au point par H.L. De Vries d'un procédé très sensible de mesure de la radioactivité 14C des échantillons, mirent en évidence les possibilités de la nouvelle méthode de datation.
Cette méthode consiste à déterminer la quantité de carbone 14 dans un matériau vivant, sachant que, lorsqu'un organisme vivant meurt, il cesse d'incorporer l'isotope pour au contraire commencer à en perdre. On peut ainsi déduire l'âge de ce matériau vivant à partir de la quantité restante de carbone 14. Largement utilisée en archéologie et en géologie, la technique de datation de Libby s'est révélée fiable pour des matériaux remontant jusqu'à environ 50.000 ans.
La découverte de la radioactivité naturelle a marqué un considérable progrès pour l'étude de la Préhistoire. On sait depuis environ 50 ans, que le matériel constitutif des sites archéologiques contient parfois des radioéléments dont la teneur varie avec le temps et qu'il est possible de dater des événements préhistoriques. Mais chaque isotope radioactif ne pourra être utilisé que dans une plage de temps bien définie, essentiellement en fonction de sa période de demi-vie et de sa concentration initiale.
Le radiocarbone ou 14C ou carbone 14, est l'un de ces éléments radioactifs. Bien qu'en faible teneur dans la nature, sa découverte a été déterminante pour l'étude d'une période de la Préhistoire limitée aux 40 ou 50 derniers millénaires.
A la suite des découvertes de Libby, grâce aux travaux des laboratoires et à l'archéologie de terrain, la datation par radioactivité est devenue une technique bien maîtrisée et employée très fréquemment pour la datation d'objets divers.
D'où vient le Carbone 14 ?
Le Carbone 14 est un isotope radioactif du « Carbone normal » que l'on trouve partout sur Terre. Le C14 ne se trouve donc qu'en très petite quantité dans la nature. Nous allons voir où et comment ce Carbone 14 est formé sur Terre, et pourquoi, malgré sa rareté, il est présent dans tous les organismes vivants.
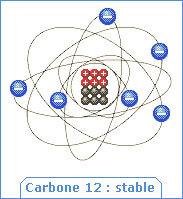
Quand on parle du Carbone, on pense a priori au Carbone 12, qui est le plus courant dans la nature. Stable et non radioactif, il est constitué de 6 électrons tournant autour d'un noyau de 6 neutrons et 6 protons (6+6=12 éléments dans son noyau d'où le nom de carbone 12). Mais, il existe aussi deux autres « formes » de Carbone, que l'on appelle ses isotopes : le Carbone 13 qui est stable lui aussi, et le Carbone 14 qui est instable et radioactif. Chacun de ces isotopes comporte 6 protons dans son noyau (sinon, ce ne serait plus du carbone...) mais le Carbone 13 a 7 neutrons et le Carbone 14 en a 8.
Dans la nature, on trouve 98,89% de Carbone 12, 1,1% de Carbone 13 et 1,2.10-12 % de carbone 14. Le carbone 14 est issu de l'azote de l'air qui entre en collision avec les neutrons créés dans l'atmosphère par les rayons cosmiques. Cette réaction de formation du carbone 14, établie en 1946 par Willard Franck Libby, est la suivante : un neutron frappe un atome d'azote (noté "N", qui a 7 protons, 7 neutrons), il rentre dans le noyau et en expulse un proton, et il reste un atome de carbone, avec 6 protons et 8 neutrons, et un proton qui se "promène tout seul".
C'est ainsi qu'une partie des neutrons créés dans l'atmosphère par les rayons cosmiques interagissent avec l'azote pour former cet isotope radioactif du carbone selon cette réaction:
14N(n,p)14C
(Réaction mise en évidence par W.F. LIBBY en 1946).
(Réaction mise en évidence par W.F. LIBBY en 1946).
Plus précisément, les protons cosmiques d'origine galactique sont plus ou moins déviés par le champ magnétique terrestre. Ceux qui pénètrent dans l'atmosphère donnent naissance à des neutrons sur les molécules d'oxygène et d'azote de l'air. Après leur production, ces neutrons entrent en collision avec les molécules de l'air; à la suite de nombreux chocs, ils sont ralentis et atteignent peu à peu l'énergie thermique des gaz. Ils donnent alors, avec une probabilité quasi-totale, du carbone 14 sur l'azote de l'air. La réaction est la suivante:
146C -> ß- + 147N
Le maximum d'intensité des neutrons secondaires se produit dans une bande d'altitude correspondant à des pressions résiduelles de 75 à 120 g/cm2 (soit de 18 à 15 km d'altitude). On retrouve le même maxi dans le spectre de taux de production du 14C. Le flux cosmique primaire est largement modulé par le champ magnétique terrestre et aussi par le champ magnétique du vent solaire interplanétaire. Il en est de même pour la production du 14C qui est affectée des mêmes variations spatiales et temporelles que le flux de protons. Elle varie d'un facteur 4 à 5 entre l'équateur et le pôle et subit des fluctuations notables au cours d'un cycle solaire (Un cycle solaire dure 11 ans).
Ceci a pour conséquence de rendre difficile le calcul exact du taux de production du 14C (teneur en 14C dans l'atmosphère).
A la suite de mesures de flux de neutrons thermiques faites en ballon à l'aide de compteurs à BF3, Richard LINGENFELTER (University of California) et Reuven RAMATY (NASA's Goddard Space Flight Center), ont calculé (1970) les taux de production suivants par cm2 de surface terrestre et par seconde:
Pour le minimum solaire
enregistré dans les années 1953-1954 :
0,91 atome de 14C cm-2 sec-1 à l'équateur,
4,99 atomes de 14C cm-2 sec-1 aux pôles.
Pour le maximum solaire
enregistré dans les années 1957-1958 :
0,86 atome de 14C cm-2 sec-1 à l'équateur,
3,50 atomes de 14C cm-2 sec-1 aux pôles.
Des calculs plus récents
faits pour le cycle solaire entre 1965-1975
(Serge A. KORFF et Rosalind B. MENDELL, 1980)
confirment et précisent ces valeurs.
Ils conduisent à un taux de production moyen de :
2,25 ± 0.1 atomes 14C cm-2 sec-1.
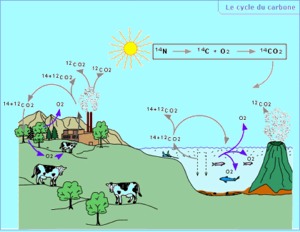
Le carbone 14 ainsi formé s'oxyde rapidement, donne une molécule de 14CO2 qui se disperse et marque de façon uniforme par sa radioactivité le gaz carbonique atmosphérique.
De l'ordre de 25% sur un cycle solaire de 11 ans, les variations du taux de production sont difficiles à observer car elles ne produisent pas un changement très sensible dans la concentration 14C atmosphérique.
HOUTERMANS (1966) a montré en effet qu'une variation périodique de 10 ans dans la production du 14C était atténuée d'un facteur 100. C'est bien ce qui a été trouvé en mesurant l'activité du bois prélevé dans les couches annuelles d'arbres (dendrochronologie). L'activité du carbone varie pendant un cycle solaire de 1 à 2 pour mille.
Ce carbone est rapidement oxydé pour donner du gaz carbonique (ex : absorbé par les plantes au cours de la photosynthèse). Le bois vivant contient donc toujours une certaine proportion de carbone 14, et on a constaté que cette quantité était constante dans le monde, chaque gramme de carbone contenant suffisamment d'isotopes 14C pour qu'un détecteur enregistre 13,6 désintégrations par minute et par gramme de carbone (dpm/g).
Lorsqu'un arbre est abattu, le bois cesse de vivre, le processus de photosynthèse s'arrête, et il n'y a plus absorption de gaz carbonique. L'isotope 14C est alors libre de se désintégrer sans compensation, selon la réaction suivante :
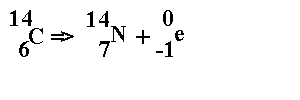
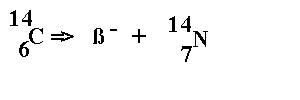
Notre arbre, comme tout matériau vivant (bois, lin, ou autre élément organique), commence alors une période de désintégration qui va permettre d'évaluer son âge, en mesurant son activité spécifique et donc son degré de radioactivité (nombre de rayons ß- émis par gramme minute par gramme de carbone) et en déduire par le calcul le temps écoulé depuis la mort de ce matériau.
Période de désintégration (demi-vie)
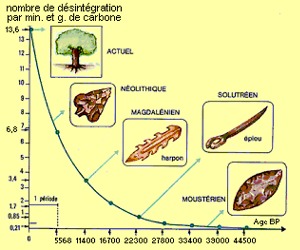
La période de demi-vie est le temps pendant lequel la moitié du Carbone 14 se désintègre. Elle est théoriquement de 5.730 ± 40 ans (GODWIN, 1962). Au bout de 5.730 ans, il y aura donc dans le matériau étudié deux fois moins de carbone 14. Suite à des conventions internationales de la communauté scientifique du radiocarbone, la période utilisée est celle mise en évidence par Willard Libby de 5.568 ± 30 ans. Valeur adoptée dès 1951 et qui continue d'être utilisée pour le calcul des âges. Le passage de cette dernière période à la nouvelle se fait en multipliant les âges par 1,03.
En appliquant les conventions internationales de la communauté scientifique du radiocarbone, on pourra donc s'attendre à ce que notre morceau de bois, au bout d'une période de 5.568 ans, n'émette plus que 6.8 électrons, ou autrement dit, qu'il ne donne que 6.8 dpm/g (désintégration par minute et par gramme).
Il est ainsi possible d'évaluer l'âge de notre spécimen de bois (ou de tout autre matériau d'origine organique, tel que par exemple le lin) d'après son degré de radioactivité.
Cette méthode de datation par le carbone 14 a été appliquée, par exemple à du bois prélevé dans des tombes égyptiennes que les archéologues estimaient vieilles de 4600 ans. On a obtenu un taux de comptage correspondant à un âge de 4500 ans, ce qui était une confirmation frappante du raisonnement des archéologues.
Formation et désintégration du carbone 14 se produisent simultanément et se conjuguent pour arriver à un équilibre radioactif qui maintient constantes la composition isotopique et l'activité spécifique du carbone atmosphérique. Cette activité naturelle est très faible, et elle a été déterminée comme étant égale à: 13,56 ± 0.07 désintégrations par minute et par gramme de carbone.
Soit 13,6 dpm/g de carbone (KARLEN et Al.,1966)
Principe de la datation
On sait que tout organisme présente de son vivant la même radioactivité que le gaz carbonique atmosphérique. A sa mort, les échanges gazeux cessent, le 14C n'est plus renouvelé, sa radioactivité décroît alors lentement à raison de la moitié tous les 5.568 ans*, c'est la période de demi-vie.
(* période adoptée par convention internationale)
Ainsi si on mesure aujourd'hui l'activité 14C = At d'un bois, on peut en la comparant à l'activité du carbone moderne Ao, en déduire le temps t qui s'est écoulé depuis sa mort. C'est ce que l'on appelle l'AGE.
L'âge s'obtient à partir de la décroissance exponentielle radioactive:
| At = Ao . e-lembda.t | |
| At | activité carbone de l'échantillon (échantillon archéologique) |
| Ao | activité carbone moderne (échantillon standard de référence) |
| Lembda | constante de désintégration Ln2/T égale à 0.69314/T |
| T | étant la période de demi-vie du 14C utilisée par convention, soit 5.568 ans |
Si on introduit la valeur de la période dans l'équation ci-dessus, on obtient une formule simple pour le calcul des âges:
AGE = log Ao/A * 8,033 103ans
Tel est le principe de la méthode. Il repose sur l'hypothèse que la radioactivité naturelle est restée constante au moins au cours des 40.000 dernières années, autrement dit, on suppose que l'activité 14C d'organismes vivants actuellement est identique à celle des mêmes organismes il y a par exemple 10.000 ans.
Cette hypothèse n'est pas rigoureusement exacte car l'activité du carbone 14 n'a pas toujours été constante dans le temps c'est à dire qu'il y a eu des fluctuations de la teneur en 14C dans l'atmosphère, aujourd'hui quantifiées et qui sont introduites dans les procédures de calibration des âges de radiocarbone.
(Cf: chapitre sur la calibration des dates.)
Le principe de la méthode de datation par le 14C consiste donc à mesurer l'activité spécifique d'un échantillon, qui est le nombre de rayons ß- émis par gramme de carbone et par minute, et en déduire par le calcul, le temps écoulé depuis la mort de l'organisme sur lequel l'échantillon a été prélevé.
La découverte de W.F. Libby, qui lui valut l'attribution du prix Nobel de Chimie en 1960, fut d'expliquer la teneur en 14C de toute matière carbonée. W.F. Libby montra que le bombardement de l'azote par des neutrons se produisait de façon continue dans la nature et que le produit de cette réaction, le radiocarbone, faisait partie intégrante de certaines matières carbonées de la nature.
Distribution du Carbone dans la nature
Bien que la production de radiocarbone soit continuelle comme l'est depuis des millénaires le rayonnement cosmique, il n'y a pas accumulation de carbone 14 parce que cet isotope est radioactif. Cela veut dire que tous les atomes de radiocarbone se désintègrent spontanément au bout d'un certain temps en émettant un électron et en redonnant un atome de 14N.
Cette désintégration est un phénomène régi par les lois de la statistique, et si l'on fait la moyenne pour un très grand nombre d'atomes, sa fréquence est absolument constante et elle est définie par la période de l'isotope 14C qui a été mesurée par les physiciens. Ces derniers ont démontré que toute matière carbonée isolée de la source de production de radiocarbone perd la moitié de sa teneur originelle en 14C et que la concentration de cet isotope diminue de moitié tous les 5.568 ans. (Convention internationale, ou 5.570 ans).
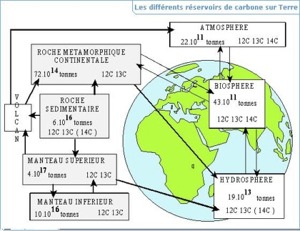
Parmi les éléments présents à la surface de la terre, le carbone est l'un des plus importants. Il est très diversement réparti :
- sous forme de gaz carbonique dans l'atmosphère (12CO2, 14CO2),
- sous forme de composés organiques dans la biosphère terrestre et marine,
- sous forme de gaz carbonique, de bicarbonates dissous et de carbonates dans les océans.
Des échanges constants de carbone se produisent dans ce système qui constitue le système échangeable.
La répartition du carbone dans l'atmosphère est connue avec une bonne précision.
C'est dans la biosphère terrestre qui comprend la matiére végétale vivante et morte, c'est à dire les végétaux et les sols, que l'on a le moins d'information.
Le carbone est, par ailleurs, beaucoup plus abondant dans le système sédimentaire constitué par les roches sédimentaires calcaires, les sédiments marins, les charbons et le pétrole. Dans les roches de formation très ancienne, le carbone est totalement dépourvu de 14C (exemple donné pour quelques millions d'années).
Les différents réservoirs sont supposés en équilibre réciproque vis à vis de la teneur en 14C qui est elle-même homogène dans chacun d'entre eux, et elle est considérée comme constante puisque l'équilibre radioactif est atteint (taux de production = taux de désintégration).
L'équilibre est rompu lorsque cesse l'interconnexion de l'un des réservoirs et seule la décroissance radioactive se produit dans le réservoir isolé.
Il est donc possible de connaître le moment où le réservoir a été isolé, donc de dater cet événement, à condition que l'échantillon n'ait pas à nouveau participé ultérieurement au cycle du carbone.
A la surface des océans la plus grande partie du carbone présent dans l'air s'échange avec celui dissous dans les eaux marines et entre dans la constitution des organismes marins; l'autre partie, par la photosynthèse, constitue les cellules de tous les organismes terrestres.
Pour que l'activité spécifique de 13,6 dpm/g de carbone reste constante, il faut que le système d'échange matiére carbonée-atmosphère reste ouvert. S'il se ferme pour une cause quelconque, telle que la mort de l'organisme ou la précipitation de calcaire, la teneur en 14C va immédiatement commencer à décroître et continuera à le faire régulièrement jusqu'à la disparition totale des isotopes radioactifs qui ne sont plus renouvelés.
Donc la teneur en radiocarbone sera d'autant plus basse qu'il se sera écoulé plus de temps depuis l'interruption de l'échange avec la source de radiocarbone.
| DATER UN ECHANTILLON PAR LE RADIOCARBONE CONSISTERA DONC A MESURER SA TENEUR EN 14C ACTUELLE ET LA COMPARER A CELLE QU'IL AVAIT LORS DE SA FORMATION. |
Le carbone 14 permet de dater un nombre considérable d'éléments et d'objets émanant d'époques très diverses. Mais, nous le verrons par la suite, ces méthodes ont leurs limites, et tout objet n'est pas forcément datable de manière fiable et efficace.
REALISATION D'UNE DATATION
Dans cette partie on décrit la réalisation d'une datation dans un laboratoire spécialisé tel qu'il en existe plusieurs dans le monde. Il s'agit ici du Centre de Datation au Radio Carbone (C.D.R.C.) de Lyon (France) où travaille Jacques Evin.
Réception des échantillons
Les échantillons reçus par les laboratoires sont nombreux, et il nécessaire de disposer d'une salle pour tous les entreposer sans danger. Dans cette pièce l'on peut trouver du charbon de bois, des os, des tourbes et des coquillages, ou même des huiles essentielles, et des produits chimiques divers, alcools, vinaigres.
Nettoyage des échantillons
Tous les échantillons reçus par le laboratoire ont une très longue histoire, et contiennent forcément beaucoup de matières qu'il est nécessaire de nettoyer : les carbonates et matières humiques sont enlevés et l'échantillon est alors prêt à brûler. Les nombreuses paillasses sont couvertes de divers bocaux entreposés depuis parfois plusieurs semaines, qui reposent et se « lavent ». La taille des échantillons est variable: des quelques milligrammes du grain de blé, aux quelques grammes du charbon de bois, ou même aux kilogrammes du fémur ou du tibia humain.
Cette phase de préparation est fondamentale dans la mesure de datation. Si elle est mal effectuée par le laboratoire, toutes les mesures peuvent être faussées.
Combustion et synthèse chimique
Une fois sortis de la salle de nettoyage, les échantillons sont parfaitement propres, et le carbone 14 qui les compose est prêt à être extrait pour réaliser les expériences. Les diverses étapes de séparation varient selon le poids des éléments, il faut donc disposer du matériel adéquat, ou alors travailler avec d'autres laboratoires du monde entier disposant du matériel nécessaire.
Par exemple, pour les petits échantillons, voici le protocole explicatif de la séparation du carbone 14 (d'après une parution du CDRC) :
On le place dans un tube de quelques centimètres contenant de l'oxyde de cuivre. L'échauffement de ce minéral à plusieurs centaines de degrés, libère de l'oxygène qui transforme en gaz carbonique tout le carbone de l'échantillon. On nettoie ce gaz en le faisant passer dans plusieurs tubes de nettoyages sur le banc, et, en fin d'opération, on l'amène dans une ampoule qui est scellée au chalumeau. Cette ampoule sera ultérieurement envoyée à un accélérateur de particules (le Centre de Lyon travaille avec les accélérateurs d'Oxford et de Groningue), grosses machines de physique, qui après accélération des ions, peuvent séparer le Carbone 14 des deux autres isotopes de carbone, le Carbone 12 et le Carbone 13. Cette manière de mesurer la teneur en radiocarbone a été développée dans plusieurs pays dont la France.
Comptage et calculs
La mesure consiste à placer dans un compteur un poids de 3,5200 g (donc précis à 0,1 mg près) de benzène préparé à partir de léchantillon. Une très petite quantité dun produit organique, (dit mélange scintillant) est ajouté, et permet de détecter chaque désintégration de radiocarbone par un petit éclair de lumière que déclenche la particule émise. Cet éclair lumineux est transformé en une impulsion électrique et le compteur accumule les informations recueillies. Il les traduit en « dpmg » (désintégration par minute et par gramme), propre à chaque échantillon mesuré.
Toutes les informations recueillies sont ensuite centralisées dans un ordinateur qui calcule alors lâge de chaque échantillon mesuré. Après quelques jours d'acquisition de données on obtient donc ainsi l'âge précis de chaque échantillon.
Publications des résultats
Tous les laboratoires publient régulièrement des documents explicatifs et mettent ainsi leur savoir à disposition des scientifiques du monde entier.
APPLICATIONS DES DATATIONS
Quel type d'objets peut-on dater ?
En théorie, tout organisme vivant (ou l'ayant été pendant un temps) est constitué d'atomes de carbone, en quantité variable selon l'espèce. Nous avons vu que, dans cet organisme, il existait un certain nombre d'atomes de carbone 14. Ce nombre augmente toute la vie durant, par l'ingérement de nourriture organique (et par conséquent chargé en carbone 14) et cet accroissement n'est stoppé que lorsque survient la mort. La quantité de carbone cesse d'être renouvelée et entre dans une phase décroissante bien précise: au bout d'une période de désintégration (5730 ans), la teneur en carbone 14 a diminué de moitié ; deux périodes plus tard, cette quantité a encore été divisée par deux, etc.
C'est sur cette constatation que le physicien Willard Libby initia en 1948 des recherches afin de rendre possible une datation à travers l'étude de la proportion de l'isotope 14 au sein des atomes de carbone.
Dent de Otodus obliquus (=Lamna obliqua)
provenant de Khouribga (Maroc) et datant de l'éocène
(Hauteur: 5 cm - Collection Eric Walravens).
Cette technique de datation reposant sur l'étude du carbone 14, présent chez tous les êtres vivants animaux et végétaux, on peut dater tout objet constitué de matériaux organiques à travers un échantillon de taille variable. Il est possible de dater des ossements, des objets en bois, et aussi des argiles et poteries, objets à priori minéraux, mais dont la composition recèle souvent des traces de matériaux végétaux (souvent désagrégés).
Quels en sont les contraintes ?
Il existe une contrainte à laquelle les scientifiques et archéologues sont obligés de se plier : c'est la taille de l'échantillon. Il doit en effet être de taille suffisante afin que l'expérience puisse être réalisable et offre des résultats probants. Parfois, notamment lors de la datation de pigments provenant de peintures rupestres, ou encore, comme ce fut le cas lors de la datation du Suaire de Turin, l'échantillon mis à la disposition des scientifiques est très mince. On est alors contraint d'utiliser des techniques plus pointilleuses, dont la plus performante est le spectromètre de masse. Ce procédé permet ainsi de réaliser les expériences avec une masse d'échantillon divisée parfois par dix, tout en gardant, bien entendu, une fiabilité importante.
Un second facteur qui influe logiquement beaucoup dans la réalisation d'une datation : le temps. En effet, sorti d'une fourchette d'âge, le comptage des isotopes est rendu très difficile. Si l'objet est par exemple très vieux, de l'ordre de 45.000 années, le nombre de désintégrations est alors extrêmement faible, et par conséquent, leur bruit s'en trouve quasiment inaudible aux appareils de mesure traditionnels (compteurs Geiger et Müller).
A l'inverse, lors de la datation d'un objet récent (moins de 1 000 ans), le bruit des désintégrations est alors trop faible pour être significatif. Heureusement, dans ce cas, grâce à l'emploi d'appareils récents, tels que le spectromètre de masse à accélérateur, les mesures demeurent tout de même fiables.
Cône, pomme de pin fossile datant du pléistocène
(entre 80.000 à 120.000 ans) provenant de Zemst, Belgique
(Hauteur: 3 cm - Collection Michèle Loneux).
Nécessité d'analyse complémentaire
De manière générale, la datation par carbone 14 nécessite souvent une analyse complémentaire, réalisée, soit par une méthode similaire mais en employant un autre élément, soit par l'intermédiaire d'une autre méthode telle que la thermoluminescence.
Grâce au carbone et à son isotope 14, on estime fiable la datation d'un objet à partir de l'an 1000 jusqu'à celle d'un objet contemporain à la grotte Chauvet-Pont d'Arc (France), c'est à dire plus généralement jusqu'à -50.000 ans. En deçà ou au delà de cette période, l'expérience est toujours réalisable, mais les conditions de celle-ci risquent d'être désastreuses et le résultat n'aura sans doute aucune valeur du point de vue scientifique. On peut néanmoins avoir recours à d'autres isotopes qui ont une période de désintégration plus ou moins importante (selon le cas). Ainsi, grâce à cette alternative, il est possible de dater des objets de toutes époques, et même extrêmement récents (certains éléments ont en effet une période de désintégration de l'ordre de quelques secondes...).
LIMITES DE LA METHODE
La teneur en C14 est-elle toujours constante ?
Contrairement à ce que l'on considère lors des datations, la teneur en carbone 14 de la planète a évoluée au cours du temps. En effet, deux phénomènes récents ont influencé cette concentration :
- de la moitié du 19ème siècle jusqu'en 1930, la combustion massive dans les industries (époque des révolutions industrielles) de carbone fossile non actif (pétrole, charbon) ont fait diminuer de 4% cette teneur.
- depuis 1955, les essais nucléaires ont complètement faussés ces chiffres, en chargeant les océans de 14C : « On ne peut aujourd'hui déterminer les périodes des réservoirs qu'à partir de mollusques prélevés vivants avant 1955, année au cours de laquelle les essais ont commencé », explique Roger McNeely (responsable du laboratoire radiocarbone à la Commission géologique du Canada (CGC).
Ces erreurs de mesure se vérifient en datant un arbre à l'aide de la méthode de dendrochronologie, qui consiste à compter les anneaux des arbres, et en comparant aux résultats du carbone 14 : les différences atteignent jusqu'à 20%. Ainsi pour corriger cette erreur, on vieillit les âges obtenus de 10%, ce qui correspond à 2.000-3.000 ans pour une période de -30.000 à -20.000 ans.
Méthode infaillible ?
Jusqu'à une époque très récente, la datation par radioactivité était considérée par la communauté scientifique et par le grand public, comme une technique extrêmement précise. Tellement précise qu'elle passait même pour être, les imprécisions de l'expérience mis à part, une méthode quasiment infaillible (dans l'absolu, scientifiquement, la fiabilité ne peut être totale, d'où le mot : « quasiment »).
Mais de nombreuses controverses apparaissent dans le cadre de certaines datations célèbres, remettant en cause l'extrême précision de cette technique. Sa fiabilité est donc de plus en plus contestée.
LE CAS DU SUAIRE DE TURIN
La datation C14 appliquée au Suaire de Turin
La datation par le Carbone 14 est une méthode très utile en archéologie et en histoire. Pour de nombreux chercheurs et pour le grand public, elle a été utile pour clore certains débats. C'est ainsi que le suaire de Turin qui aurait servi à ensevelir le corps du Christ a été daté en 1988, par trois équipes indépendantes, dans une fourchette d'âge entre 1260 et 1390 ans, donc, d'après de nombreux chercheurs, un suaire fabriqué au Moyen-Âge.
En 1979, le chef d'un groupe de recherche italien, le prof. Pierluigi Bollone déclarait : « selon ce qui semble être une opinion largement répandue, profondément enracinée mais totalement sans garantie, le test au carbone 14 résoudrait certainement tous les doutes au sujet de l'authenticité de la célèbre relique. Mais on obtiendrait pas la vérité. . . cela ne nous dirait rien sur la nature de ses images mystérieuses. »
Bollone avait raison naturellement : une datation authentifiant le suaire n'aurait rien prouvé, alors qu'une datation postérieure discrédite le suaire. Cette opinion est partagée par Jacques Évin, directeur du centre de datation radiocarbone à l'université Claude-Bernard de Lyon 1, et ferme défenseur de la validité de la datation obtenue en 1988 : « La datation n'apporte rien quant à la connaissance de la manière par laquelle l'image s'est produite » {Le Monde, 16 avril 1998).
Une affaire très controversée
L'affaire du Suaire de Turin est l'exemple le plus évident de l'incertitude qui plane autour de la méthode de datation par le C14. Contrairement à d'autres datations telles que par exemple celles des tombes de l'antique Egypte citées plus haut, celle du Suaire n'est pas du tout en corrélation avec son histoire connue. On trouve en effet des traces historiques du trajet du Suaire en Orient bien avant la période 1260 - 1390 trouvée par la datation au C14.
Entre le début du 5ème siècle et 944, différents historiens de l'époque ont écrit qu'il était connu sous le nom de Mandylion et qu'il se trouvait à Edesse (Turquie orientale). Plus tard, à Constantinople entre 944 et 1204 au cours des croisades, plusieurs témoins l'ont vu et décrit alors qu'il était exposé en public. Enfin, des récits signalent sa présence à l'Acropole en 1205 dans les mains du duc d'Athènes.
Par ailleurs, la plupart des scientifiques sont d'accord, il ne peut s'agir d'un tableau. Les analyses pigmentaires ont démontré qu'aucune trace de peinture n'était présente dans la coloration du Suaire. Toutes les analyses effectuées, de la plus récente à la plus ancienne n'ont trouvé que des traces de sang humain. Normalement, un tableau présente à l'analyse fine (au microscope à balayage, par exemple) des traits de pinceaux ou même de doigts, or l'image du Linceul est totalement isotrope. Sur un tableau il y a généralement plusieurs couches de peinture, ou celle-ci est diluée par endroits, plus épaisse à d'autres. Ici, rien de tel. Sur toute l'image, la coloration a la même superficialité, elle atteint seulement la partie supérieure de la fibre. Les intensités sont dues au plus grand nombre de fibrilles coloriées.
D'autres constats excluent presque définitivement l'hypothèse d'un tableau : les examens pratiquées par des médecins anatomistes ont en effet conclu à une parfaite reproduction d'un corps humain portant les marques du supplice de crucifixion. Les scientifiques ayant réalisé ces examens ont précisé à l'issue de leur analyse que la perfection de la reproduction incluait des détails (notamment au niveau de l'agencement des os des pieds et de leur déformation suite au supplice) totalement inconnus à l'époque, si l'on en croit les traités de médecine parus au moyen âge.
En fait le seul moyen d'obtenir sur une toile de lin comme le Suaire une pareille pigmentation nécessite soit l'exposition prolongée à un flux de protons, technique n'existant pas au Ier comme au XIVè Siècle, soit l'embaumement d'un corps ensanglanté ou recouvert d'une substance azotée. Mais là encore, l'hypothèse demeure improbable. En effet, comment le faussaire aurait-il pu retirer le corps, à la suite de la pigmentation, sans laisser de traces de cette manipulation ?
Le tissu lui même apporte des éléments qui peuvent appuyer certaines thèses. C'est une toile de lin identique à celle qu'utilisaient les juifs pour l'embaumement des défunts aux premiers siècles. Une étude plus approfondie révèle que le tissu, a été tressé puis teint, et non l'inverse, comme cela se pratiqua jusqu'au 8e Siècle. Il est clair qu'un faussaire du Moyen-Âge ne peut avoir réalisé pareille imitation.
Devant l'accumulation de tous ces éléments, on peut supposer que la datation au carbone 14 est erronée, puisqu'elle entre alors en contradiction avec la quasi-totalité des précédentes analyses.
On peut bien sûr penser à une défaillance humaine : si l'échantillon à dater n'a pas été correctement nettoyé, il est possible que subsistent de petits éléments extérieurs tels que des poussières, qui peuvent fausser la mesure. Mais l'erreur mise à part, on peut constater que, de manière générale, une datation au carbone 14 n'est jamais fiable à 100%. L'imprécision est parfois minime (environ 5% pour les plus précises), mais, étant donné l'important âge des échantillons, cette erreur peut parfois représenter plus de neuf siècles. D'où la prudence avec laquelle il faut parfois interpréter ce genre de résultats.
Cette méthode repose sur le calcul de la proportion 14C/12C. On a longtemps considéré que la désintégration se faisait de manière régulière. Or, depuis quelques années, les scientifiques ont constaté que cette désintégration n'était pas toujours régulière. Il a donc fallu réétaloner les tables qui mettent en parallèle la proportion de carbone 14 encore présent dans l'échantillon et l'âge de celui-ci.
On a pu également constater à travers la datation de plusieurs objets que la variation naturelle du champ magnétique de la Terre peut, bien qu'étant très minime, influer sur la désintégration des atomes de carbone 14 en atomes de carbone 12 (tout comme la température peut également jouer un rôle). D'autres hypothèses existent. La présence de microchampignons dans le tissu pourrait l'avoir "rajeuni" aux yeux du spectromètre de masse. Seule une étude poussée permettrait de valider cette idée.
Quelles peuvent être les causes
des erreurs de datation ?
Les différents incendies subis par le Suaire au cours des siècles ont très bien pu recharger le tissu en carbone 14, faussant ainsi les mesures effectuées ultérieurement. Ce phénomène a pris, ces cinquante dernières années, une ampleur considérable du fait de l'activité humaine. La pollution et plus particulièrement le rejet dans l'atmosphère d'énormes quantités de dioxyde de carbone ont faussé de manière très significative les mesures réalisées sur des objets plus contemporains.
De même, les nombreux essais nucléaires atmosphériques réalisés dans les années cinquante et soixante ainsi que les incidents du nucléaire civil (Tchernobyl, Harrisburg...) ont fait considérablement varier la proportion 14C/12C (on estime que les essais sur la bombe H réalisés en 1962 ont fait doubler en un an la teneur en 14C de l'atmosphère terrestre). Même les appareils de mesure peuvent être perturbés par la radioactivité ambiante, rendant alors les mesures hasardeuses. Ce phénomène pourrait être accentué par la faible taille de l'échantillon fourni à l'équipe scientifique, du fait de la valeur symbolique que ce tissu a pour les chrétiens.
DATATION D'AUTRES RELIQUES
La datation appliquée à d'autres reliques
Un autre objet a été ainsi sujet à débat: il s'agit de la Chaire de Pierre au Vatican. D'après la tradition il s'agirait du « trône épiscopal de St Pierre », (appelé ainsi depuis 1230), mais ceci a été rejeté. Le bois de cette Chaire a lui aussi été daté du Moyen-Age. En fait, cette Chaire, qui est maintenant enchassée dans un reliquaire Bernini, est constituée de plusieurs bois diversement datés des 4ème-6ème et 10ème-12ème siècles. Elle est probablement l'oeuvre d'artisans païens et a sans doute été reconvertie plus tard à un usage lithurgique.
Un fragment de la vraie croix, placé dans le Triptyque de Stavelot, collection Pierpont Morgan, New York, est daté de 595±115. (Calvin disait qu'il y avait assez de ces fragments pour construire « un bon bateau ». Un calcul de 1870 estime le volume de la croix à 178 millions de millimètres cubes sur lesquels 4 millions existeraient sous forme de reliques, les 174 millions restant ayant succombés aux processus taphonomiques). Chez Pierpont Morgan se trouve aussi un morceau de la robe de la Vierge daté du 13ème siècle par le radiocarbone.
Aucun suaire auparavant n'a été daté au radiocarbone. La réputation du suaire de Cadouin en France, le principal concurrent du précédent, n'a pas été remise en cause depuis 1934, alors qu'il semble avéré qu'il ait été tissé en Egypte au 10ème siècle après JC. Il contient en effet des bandes ornementales brodées bénissant Allah en caractères coufiques. Il y a aussi des tuniques rivales de la passion à Argenteuil et à Trèves, ainsi qu'un autre suaire à Besançon. Des essais scientifiques sur la tunique d'Argenteuil, faits avant son enlèvement par le groupe français Action Directe en 1983 (ce fut la première relique soumise à une demande de rançon terroriste), montre qu'elle a été tissée à peu près à l'époque du Christ.
En conclusion
On peut dire pour conclure que la méthode de datation au carbone 14 ne peut en aucun cas être considérée comme un moyen unique pour dater un objet. Comme nous l'avons vu dans cette petite étude il est indispensable d'une part de mettre les résultats obtenus par le C14 en corrélation avec l'histoire connue de l'objet, et d'autre part d'essayer de recouper ces résultats avec ceux que pourraient donner la dendrochronologie, la thermoluminescence, ou encore l'influence de l'électromagnétisme sur la mesure.
On peut aussi trouver tous ces sujets traités
dans des CDs disponibles sur ce site :
(1) Le Mandylion: une énigme de 2000 ans,
François Gazay, Mersi Multimedia, 2000
(2) Ordre des Templiers:
le mystérieux culte de la tête magique,
François Gazay, Mersi Multimedia, 2005
(3) La controverse de Turin: vraie Relique ou faux Suaire ?,
François Gazay, Mersi Multimedia, 2006
Pour découvrir et se procurer ces CDs, cliquer ICI.
This short study describes the theoretical principle of a radiocarbon dating, the implementation of a dating experiment, the use of this method in various application fields, and the analysis of the limits of radiocarbon dating. It is followed by a talk on the dating of Shroud of Turin and other Relics.
Within the framework of historical and scientific research of Shroud Group Science on the Shroud of Turin, we present in this study the methods used by the C.D.R.C. laboratory (Lyons, France) for the dating by radioactivity, and more particularly by Carbon-14 method.
More than a simple article, we tried to make a deepened study on this subject which is based on the documents provided by this laboratory, with the aim in view to provide a base of precise discussion to the members of Shroud Science Group.
DATING PRINCIPLE
Why the Carbon-14 ?
For several centuries already, the scientists had dated the archaeological objects according to layers in which they were discovered (stratigraphy). They compared the various beds of layers and could thus date them, the lower layers being regarded as older than the higher layers. It is with this technique that the researchers divided the history of the Earth into four great parts: Precambrian Time, Paleozoic Time, Mesozoic Time and Cenozoic Time.
With the end of the 19th century, at the time of the discovery of radioactivity by French Henri Becquerel and the French couple Pierre and Marie Curie, the possibility of using the radioactive elements for the datings started to be considered. The isotope of carbon was then discovered almost fortuitously in 1934 when an American physicist, F.N.F. Kurie, exposed nitrogen to a flow of neutrons.
But the true discovery of natural radiocarbon, goes back to 1946, when Willard Franck Libby, an American chemist, put forward the idea of a continuous production of this isotope in nature and establishes the theoretical and practical bases of its use for datings in Archaeology.
Libby showed that the tritium, isotope of hydrogen, is produced by cosmic radiations. In 1947, he developed, with his students, the technique of carbon-14 dating. He had indeed the idea to study the proportion of carbon-14 in two wooden objects coming from an Egyptian tomb, and thus carried out the first dating by radioactivity of the History and he received for it a Nobel Prize in Chemistry in 1960.
The first results of W.F. Libby in 1949 and 1950 and the development by H.L. De Vries of a very significant process of measurement of the Carbon-14 radioactivity of the samples, underscore all the possibilities of the new method of dating.
This method consists in determining the quantity of carbon-14 in an alive material, knowing that, when a living organism dies, it ceases incorporating the isotope for on the contrary starting to lose some. One can thus deduce the age from this alive material starting from the remaining quantity of carbon-14. Largely used in archaeology and geology, the technique of dating of Libby appeared reliable for materials going up until approximately 50,000 years.
The discovery of the natural radioactivity marked a considerable progress for the study of Prehistory. One knows in fact, since approximately 50 years, that the material constitutive of archaeological sites contains sometimes some radioelements whose the content varies versus the time and which it is thus possible to date from the prehistoric events. But each radioactive isotope could be used only in one well defined range of time, primarily according to its period of half-life and its initial concentration.
Radiocarbon, or 14C or carbon-14, is one of these radioactive elements. Although it is only in low content in nature, its discovery was determining for the study of a limited period of Prehistory that is to say about the last 40 or 50 millenia.
Following the discoveries of Libby and thanks to the works of the laboratories together with the in-situ archaeology, the dating by radioactivity became a well controlled technique and very frequently employed for the dating of various objects.
From which does Carbon-14 come ?
Carbon-14 is a radioactive isotope of the « normal Carbon » which one finds everywhere on Earth. The C14 is thus only in very small quantity in nature. We will see in this part where and how this Carbon-14 is formed on Earth, and why, in spite of its scarceness, it is present in all the living organisms.
When one speaks about Carbon, one thinks a priori about Carbon-12, which is most current in nature. Stable and nonradioactive, it consists of 6 electrons spining round a core of 6 neutrons and 6 protons (6+6=12 elements in its core, where the carbon-12 name comes from). But, there are two other different "Carbon shapes", which one calls its isotopes: the Carbon-13 which is stable also, and the Carbon-14 which is unstable and radioactive. Each one of these isotopes comprises 6 protons in its core (if not, it would not be carbon, any more...) but Carbon-13 has 7 neutrons and Carbon-14 has 8 neutrons.
In nature, one finds 98.89% Carbon -12, 1.1% Carbon-13 and 1.2.10-12 % of Carbon-14. Carbon-14 results from nitrogen of the air which enters in collision with the neutrons created the atmosphere by the cosmic rays. This reaction of formation of carbon-14, established in 1946 by Willard Franck Libby, is as follows: a neutron strikes a nitrogen atom (noted "N", which has 7 protons, 7 neutrons), it penetrates into the core and expels a proton of it, so that with final, there remains a carbon atom, with 6 protons and 8 neutrons, and 1 proton which walks alone.
Thus a part of the neutrons created in the atmosphere by the cosmic rays interact with nitrogen to form this radioactive isotope of carbon according to the reaction given below:
14N(n,p)14C
(Reaction highlighted by W.F. LIBBY in 1946).
(Reaction highlighted by W.F. LIBBY in 1946).
More precisely, the cosmic protons of galactic origin are more or less deviated by the terrestrial magnetic field. Those which penetrate in the atmosphere give birth to neutrons on the molecules of oxygen and nitrogen of the air. After their production, these neutrons enter in collision with the molecules of the air; following many shocks, they are slowed down and reach little by little the thermal energy of gases. They give then, with a quasi-total probability, carbon-14 on nitrogen of the air. The reaction is as follows:
146C -> ß- + 147N
The maximum of intensity of the secondary neutrons occurs in a band of altitude corresponding to residual pressures from 75 to 120 g/cm2 (that is to say from 18 to 15 km of altitude). One finds the same maximum in the spectrum of production rate of the 14C. Primary cosmic flow is largely modulated by the terrestrial magnetic field and also by the magnetic field of interplanetary solar wind. It is the same for the production for the 14C which is affected by the same space and temporal variations as the flow of protons. It indeed varies by a factor 4 to 5 between the equator and the pole and it is subjected to some notable fluctuations during a solar cycle (a solar cycle lasts 11 years).
It results that it is difficult to calculate exactly the production rate of the 14C (content of 14C in the atmosphere).
Following measurements of thermal flows of neutrons made in balloon by using BF3 counters, Richard LINGENFELTER (University of California) and Reuven RAMATY (NASA' S Goddard Space Center Flight), calculated (1970) the following production rates per cm2 of terrestrial surface and per second:
For the solar minimum
recorded in the years 1953-1954:
0.91 atom of 14C cm-2 sec-1 at the equator,
4.99 atoms of 14C cm-2 sec-1 to the poles.
For the solar maximum
recorded in the years 1957-1958 :
0.86 atom of 14C cm-2 sec-1 at the equator,
3.50 atoms of 14C cm-2 sec-1 to the poles.
More recent calculations
made for the solar cycle between 1965-1975
(Serge A. KORFF and Rosalind B MENDELL, 1980)
confirm and specify these values.
They lead to an average production rate of:
2.25 ± 0.1 atoms 14C per cm2/sec-1.
Carbon-14 thus formed oxidizes quickly and gives a molecule of 14CO2 which disperses and in a uniform way marks with its radioactivity the atmospheric carbon dioxide.
Although about 25% during a solar cycle of 11 years, the variations of the production rate are difficult to observe because they do not produce a very significant change in the concentration of the atmospheric 14C.
HOUTERMANS (1966) has well demonstrated indeed that a periodic variation of 10 years in the production of the 14C was attenuated by a factor 100. It is well what was found by measuring the activity of the wood taken in the annual layers of trees (dendrochronology). The activity of carbon varies during a solar cycle from 1 to 2 per thousand.
This carbon is quickly oxidized to give carbon dioxide (eg: absorbed by the plants during photosynthesis). The alive wood thus contains always a certain proportion of carbon-14, and it was noted that this quantity was constant in the world, and consequently each gram of carbon contains a sufficient quantity of 14C isotopes so that a detector can record 13.6 disintegrations per minute and per gram of carbon (dpm/g).
When a tree is cut down, wood ceases living, the process of photosynthesis stops, and there is no more absorption of carbon dioxide. The isotope 14C is then free to disintegrate without compensation, according to the following reaction:
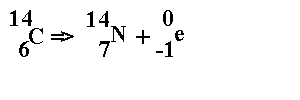
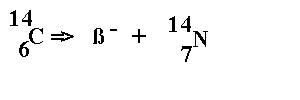
Our tree, like any alive material (wood, flax, or another organic element), then begins a period of disintegration which will make it possible to evaluate its age, by measuring its specific activity and thus its degree of radioactivity (quantity of rays ß- emitted per gram minute per gram of carbon) and to deduce by calculation the time elapsed since the death of this material.
Period of disintegration (half-life)
The period of half-life is the time during which the half of Carbon-14 disintegrates. It is theoretically of 5,730 ± 40 years (GODWIN, 1962). That is to say that at the end of 5,730 years, there will be in studied material twice less carbon-14. But following International Conventions of the radiocarbon scientific community, to avoid confusions, the period used is that was highlighted by Willard Libby i.e. 5,568 ± 30 years. This value is adopted since 1951 and which continues to be used for the calculation of the ages. The passage of this last period to the news is done by multiplying the ages by the factor: 1.03.
By applying the International Conventions of the scientific community of radiocarbon, one will be able to thus expect that our piece of wood, at the end of a period of 5,568 years, emits nothing any more but 6.8 electrons, or in other words, that it gives only 6.8 dpm/g (disintegration per minute and per gram).
It is thus possible to evaluate the age of our specimen of wood (or any other material having an organic origin, such as for example the flax) according to its degree of radioactivity.
This method of dating by carbon-14 was applied, for example with wood taken in Egyptian tombs that the archaeologists have estimated dated back to about 4600 years. One obtained a counting rate corresponding to a 4500 years age, which was a striking confirmation of the reasoning of the archaeologists.
In this way, the formation and the disintegration of the carbon-14 occur simultaneously and are combined to arrive at a radioactive balance which maintains constant the isotopic composition and the specific activity of the atmospheric carbon. Thus, this natural activity is very weak, and it was given as being equal to: 13.56 ± 0.07 disintegrations per minute and per gram of carbon.
That is to say 13.6 dpm/g of carbon (KARLEN and Al, 1966)
Dating Principle
One knows that any organism presents in its leftime the same radioactivity as atmospheric carbon dioxide. With its death, the gaseous exchange ceases, the 14C is not renewed more, its radioactivity decreases then slowly at a rate of half every 5,568 years *, it is the period of half-life.
(* period adopted by International Convention)
Thus, if one measures today the 14C activity = At of a wood, one can by comparing it with the activity of modern carbon Ao, to deduce the time t which elapsed since its death. It is what one calls the AGE.
Age is calculated from the formula of radioactive exponential decay:
| At = Ao . e-lembda.t | |
| At | carbon activity of the sample (archaeological sample) |
| Ao | activity of modern carbon (standard sample of reference) |
| Lembda | constant of Ln2/T disintegration equal to 0.69314/T |
| T | being the period of half-life of the 14C used by convention, i.e. 5,568 years |
If one introduces the value of the period into the equation above, one obtains a simple formula for the calculation of the ages:
AGE = log Ao/A * 8.033 103 years
Such is the principle of the method. It is based on the assumption that the natural radioactivity is remained constant at least during 40,000 last years, in other words, one supposes that the 14C activity of the organisms currently living is identical to that of the same organisms which lived, for example, 10,000 years ago.
This assumption is not rigorously exact because the activity of carbon-14 was not always constant in time i.e. that there were fluctuations of the content of 14C in the atmosphere, now quantified and who are introduced into the procedures of correction and calibration of the radiocarbon ages.
(See: chapter on the calibration of the dates.)
The principle of the method of dating by the 14C thus consists to measure the specific activity of a sample, which is the number of rays ß- emitted per gram of carbon and per minute, and to deduce some by calculation, the time elapsed since the death of the organism on which the sample was taken.
The discovery of W.F. Libby, ending in a Nobel Prize in Chemistry he received in 1960, was to explain the content of 14C of any carbonaceous matter. W.F. Libby showed that the bombardment of nitrogen by neutrons occurred continuously in nature and that the product of this reaction, the radiocarbon, was an integral part of certain carbonaceous matters of nature.
Distribution of Carbon in nature
Although the production of radiocarbon is continual as it is the case since millenia for the cosmic radiation, it does not have accumulation of carbon-14 there because this isotope is radioactive. That wants to say that all the radiocarbon atoms are disintegrated spontaneously at the end of a certain time by emitting one electron and by giving again one atom of 14N.
As this disintegration is a phenomenon governed by the laws of the statistics, if one makes the average for a very great number of atoms, its frequency is absolutely constant and it is defined by the period of the isotope 14C which was measured by the physicists. Those latter ones showed that all carbonaceous matter isolated from the source of production of radiocarbon loses half of its original content of 14C and that the concentration of this isotope decreases by half every 5,568 years. (International Convention, if not, it is 5,570 years).
Among the elements present at the surface of the ground, carbon is one of most important. It is very variously distributed :
- in the form of carbon dioxide in atmosphere (12CO2, 14CO2),
- in the form of organic compounds in the terrestrial and marine biosphere,
- in the form of carbon dioxide, of dissolved bicarbonates and carbonates in the oceans
Constant exchanges of carbon occur in this system which constitutes the exchangeable system.
The distribution of the carbon in the atmosphere is known with a rather good precision.
It is in the terrestrial biosphere which include the alive and died vegetable matter, i.e. the plants and the soils, which one has less information.
Carbon is, in addition, much more abundant in the sedimentary system which is composed of the sedimentary limestone rocks, the marine sediments, the coals and the oil. In the rocks of very old formation, the carbon is completely deprived of 14C (the example is given for a few million years).
The various tanks are supposed in reciprocal balance with respect to the content of 14C which is itself homogeneous in each one of them, and it is regarded as constant seeing that the radioactive balance is reached (the production rate = the disintegration rate).
Balance is broken when the interconnection of the one of the carbon tanks ceases and then only the radioactive decrease occurs in the insulated tank.
It is thus possible to know the moment when the tank was insulated, therefore to date this event, provided that the sample again did not take part later on in some way in the cycle of carbon.
At the surface of the oceans the greatest part of carbon present in the air is exchanged with that dissolved in marine water and goes into the constitution of the marine organisms; the other part, by photosynthesis, more or less directly constitutes the cells of all the terrestrial organisms.
In such a way that the specific activity of 13.6 dpm/g of carbon remains constant, it is necessary that the system of exchange carbonaceous matter - atmosphere remains open. If it is closed for some cause, such as the death of the organism or the limestone precipitation, the content of 14C immediately will start to decrease and will continue to regularly do it until the total disappearance of the radioactive isotopes which are not renewed any more.
Thus the content of radiocarbon will be all the more low as it will have elapsed more time since the interruption of the exchange with the source of radiocarbon.
| TO DATE A SAMPLE BY RADIOCARBON WILL THUS CONSIST TO MEASURE ITS CURRENT CONTENT OF 14C AND TO COMPARE IT WITH THAT IT HAD AT THE TIME OF ITS FORMING. |
Carbon-14 makes it possible to date back a considerable number of elements and objects issued from very diverse times. But, we will see it thereafter, these methods have their limits, and any object is not inevitably datable in a reliable and effective way.
DATING IMPLEMENTATION
In this part we will describe the implementation of a dating in a laboratory specialized such as it exists several in the world. It is here the Center of Radiocarbone Dating (C.D.R.C.) from Lyons (France) where Jacques Evin works.
Reception of the samples
The samples received by the laboratories are many, and it is necessary to have a room for all to store them without danger. In this room one can find some charcoal, bones for archaeology, peats and shells for the geology of quaternary, or even essential oils, various chemicals, alcohols, vinegars for the various expertises.
Cleaning of the samples
All the samples received by the laboratory have a very long history, and contain inevitably far too many matters which it is necessary to clean: some carbonates, organic materials are thus removed, and the sample is then ready to burn. The many work surfaces of the room have been covered with various bottles stored for sometimes several weeks, which settle here and « wash themselves ». The sample size is very variable, that goes from the few milligrams of the corn grain, to the few grams of the charcoal, or even to the kilogrammes of the femur or the tibia of human.
It should be known that this phase of preparation is fundamental in the measurement of dating. If it is badly carried out by the laboratory, all measurements can be distorted.
Combustion and chemical synthesis
Once left the room of cleaning, the samples are perfectly clean, and the carbon-14 which composes them is ready to be extracted to carry out the experiments. The various stages of separation vary according to the weights of the elements, and thus it is necessary to have the adequate material, or then to work with other laboratories of the whole world having the material necessary.
For example, for the small samples, here the explanatory protocol of the separation of carbon-14 (according to a publication of the CDRC):
One places the sample in a tube of a few centimetres containing some copper oxide. The heating of this mineral to several hundreds of degrees, releases the oxygen which transforms all the carbon of the sample into carbon dioxide. One cleans this gas by making it pass in several tubes of cleanings on the bench, and, at the end of the operation, one brings it in a bulb which is sealed with a blowtorch. This bulb will be sent later on to a particle accelerator (the Center of Lyons, France, works with the accelerators of Oxford, UK, and Groningen in the Netherlands), large machines of physics, which after acceleration of the ions, can separate Carbon-14 from the two other carbon isotopes, Carbon 12 and Carbon 13. This way to measure the content of radiocarbon was developed in several countries and, among others, in France.
Counting and calculations
Measurement consists in placing in a counter a weight of 3.5200 g (within 0.1 mg) of benzene prepared from the sample. A very small quantity of an organic material, (known as scintillating mixture) is added, and allows to detect each radiocarbon disintegration through a small flash of light triggered by the emitted particle. This luminous flash is transformed into a pulse (disintegration hit) and the counter thus accumulates information collected. It translates them into « dpmg » i.e. disintegration per minute and per gram, specific to each sample to be measured.
All collected information is then centralized in a computer which can instantaneously calculate the age of each measured sample. Thus it is possible to then precisely obtain the age of the sample, at the end of a few days of data acquisition.
Publications of the results
All the laboratories publish regularly explanatory documents and thus place their knowledge at the disposal of the scientists of the whole world.
DATING APPLICATIONS
What type of objects can be dated ?
In theory, any alive organism (or having been it during a time) consists of carbon atoms, in variable quantity according to the species. We saw previously that, in this organism, there was a certain number of carbon-14 atoms. This number increases all the life during, by ingestion of organic food (and consequently charged out of carbon-14) and this increase is stopped only when death occurs. The quantity of carbon then ceases being renewed and enters then in a decreasing phase according to a quite precise proportion: at the end of one period of disintegration (5,730 years), the carbon-14 content decreased by half; two periods later, this quantity was still divided by two and so on.
It is on this observation that in 1948 the physicist Willard Libby initiated a research in order to make possible a dating through the study of the proportion of the isotope 14 within the carbon atoms.

Tooth of Otodus obliquus (= Lamna obliqued)
coming from Khouribga (Morocco) and dating from the Eocene
(Height: 5 cm - Collection Eric Walravens).
Knowing that this dating technique is based on the study of carbon-14 present in all alive organisms like animals and plants, in theory, one can thus date any object made up of organic materials through a variable sample of size. Thus, it is possible to date from some bones or wooden objects, but also from the clays and the potteries, objects a priori mineral, but whose composition often contains some traces of vegetable material (often disaggregated).
What are the restraints ?
There is in addition a constraint to which the scientists and archaeologists are obliged to yield: the size of the sample. This one must indeed be of sufficient size so that the experiment can be realizable and offers convincing results. Sometimes, in particular at the time of the dating of pigments coming from cave paintings, or, as it was the case at the time of the dating of the Shroud of Turin, the sample placed at the disposal of the scientists is very thin. One is then constrained to use more specific techniques, the most powerful of which being the mass spectrometer. This process thus makes it possible to carry out the experiments with a quantity of sample divided sometimes by ten, while keeping the same reliability.
A second factor which logically influences much in the realization of a dating: the time. Indeed, apart from an age range, the counting of the isotopes is very difficult to do. If the object is for example very old, about 45,000 years, the number of disintegrations is then extremely weak, and consequently, their noise is some almost inaudible with the traditional measuring intruments (Geiger-and-Müller counters).
Conversely, at the time of the dating of a recent object (less than 1,000 years), the noise of disintegrations is then too weak to be significant. Fortunately, in this case, thanks to the use of recent instruments, such as the accelerator mass spectrometer, the measurements all the same remain reliable.

Fossil pine cone dating from pleistocene
(between 80,000 to 120,000 years) coming from Zemst, Belgium
(Height: 3 cm - Collection Michele Loneux).
Necessity for a complementary analysis
In a general way, the dating by carbon-14 often requires a complementary analysis, carried out, either by a similar method but by employing another element, or by the intermediary of another method such as thermoluminescence.
Thanks to carbon and its isotope 14, one considers reliable the dating range from an object dated back to the year 1000 to an object contemporary with the cave Chauvet-Pont d'Arc (France), that is to say more generally, dated back to -50,000 years. Before or after this time range, the experiment is always realizable, but the conditions of the measurement will be distrasous and the result will not undoubtedly have any value from the scientific point of view. One can nevertheless have recourse to other isotopes which have a period of disintegration more or less important (according to the case). Thus, thanks to this alternative, it is possible to date objects of all times, and even extremely recent (certain elements indeed have a period of disintegration of the order of a few seconds...).
DATING LIMITS
Is the content of C14 always constant ?
Unfortunately, and as opposed to what one considers at the time of the datings, the content of the carbon-14 of the planet has varied versus time. Indeed, two recent phenomena influenced this concentration:
- from the half of 19th century to 1930, massive combustion in industries (period of industrial revolution) of nonactive fossil carbon (oil, coal) made decrease by 4% this content.
- since 1955, the many nuclear tests completely distorted these figures, by charging the oceans of 14C: « One can thus today determine the periods of the carbon tanks only starting from molluscs taken alive before 1955, year during which the tests have started », explains Roger McNeely (responsible for the laboratory of radiocarbon at the Geological Commission of Canada (CGC).
These errors of measurement are checked by dating a tree using the method of dendrochronology which consists in counting the rings of the trees, and by comparing with carbon-14 results: the differences reach up to 20%. Thus, to correct this error, one makes 10% older the ages obtained, i.e., which corresponds to a correction of 2,000-3,000 years for a period of -30,000 to -20,000 years.
Infallible method ?
Up to one time still very recent, the method of dating by radioactivity was regarded by the scientific community, and general public in a general way, as an extremely precise technique. So much precise that it even considered to be, the inaccuracies of the experiment put aside, like an almost infallible method (in the absolute, scientifically speaking, reliability cannot be total, from where the use of the word: « almost »).
But increasingly many controversies appear within the framework of certain famous datings, calling into question the extreme precision of this technique. Its reliability thus is disputed more and more.
DATING OF TURIN SHROUD
The dating method applied to the Turin Shroud
The dating by Carbon-14 is a very useful method in archaeology and history. For many researchers and general public, it was useful to close certain debates. Thus the shroud of Turin which would have been used to bury the body of Christ was dated in 1988, by three independent teams, in an age range between 1260 and 1390 years, therefore, according to many researchers, a shroud manufactured in the Middle Ages.
The leader of an italian search team, Prof. Pierluigi Bollone, said in 1979, « according to what appears to be a widely diffused, deeply rooted but totally unwarranted opinion, the Carbon 14 test would.., definitely solve all doubts concerning the authenticity of the famous Relic. Nothing is further from the truth . . . it would tell us nothing about the nature of its mysterious images. »
Bollone is right of course: a date compatible with authenticity of itself proves nothing, while any later date rules out the Shroud. This opinion is shared besides by Jacques Évin, director of the center of radiocarbon dating (C.D.R.C.) at the university Claude-Bernard of Lyon 1, and firm defender of the validity of the dating obtained in 1988 : « the dating does not bring anything to the knowledge about the manner by which the image occurred » {Le Monde, April 16, 1998).
A very discussed affair
The affair of the Shroud of Turin is the most obvious example of the uncertainty which planes around the method of dating by the C14. Indeed, contrary to other datings such as for example those of the tombs of the antique Egypt referred to above, that of the Shroud is not at all in correlation with its known history. One indeed finds historical traces of the way of the Shroud in the Orient well before the period 1260 - 1390 found by the dating with C14 method.
Between the 5th century and 944, historians of the time wrote that the Shroud was known under the name of Mandylion and it was in Edessa (Eastern Turkey). Later, in Constantinople between 944 and 1204 during crusades, several witnesses saw and described it whereas it was displayed to the public. Lastly, some accounts announce its presence to the Acropolis in 1205 in the hands of the duke of Athens.
In addition, the majority of the scientists agree, it cannot be a painting. The pigmentary analyses indeed showed very early that no trace of painting was present in the colouring of the Shroud. All the analyses carried out, from the most recent to the oldest found only traces of human blood. Normally, a painting present under fine analysis (under the scanning electron microscope, for example) the features of brushes or even of fingers, but the image of the Shroud is completely isotropic. Moreover, on the paintings, there are generally several coats of paint, or then this one is diluted by places, thicker with others. Here, nothing like it. On all the image, the colouring has the same superficiality, it reaches only the higher part of linen fibre. The intensities are due to the greatest number of colored fibrillae.
Other reports almost definitively exclude the assumption from a painting: the examinations practised by the anatomists thus concluded with a perfect reproduction from a human body carrying the marks of the crucifiction supplice. The scientists having carried out these examinations specified at the analysis end that the perfection of the reproduction included details (in particular on the level of the fitting of the bones of the feet and their deformation following the suplice) completely unknown at the time, if one believes the treaties of medicine published during the Middle Ages.
The only means of obtaining on a linen fabric as the Shroud a similar pigmentation requires either a prolonged exposure to a flow of protons, technique not existing in the 1st century and in the 14th century, either the embalming of a blood-soaked body or covered with a nitrogenized substance. But there still, the assumption remains improbable. Indeed, how the forger could have withdrawn the body, following the pigmentation, without leaving traces of this handling ?
The fabric itself brings elements which can support some theories. It is indeed a linen cloth identical to that the Jews used for the embalming of the dead during first centuries of our era. A thorough study reveals moreover that this fabric was braided then dyed, and not the reverse, as that was practised until 8th century. It appears clear that a forger of the Middle Ages cannot have carried out similar imitation.
In front of the accumulation of all these elements, one can suppose that the dating with carbon-14 is erroneous, since it enters then in contradiction with the near total of the preceding analyses.
One can of course think of a human failure: if the sample to be dated were not beforehand properly cleaned, it is possible that small external elements remain such as dust particles, which can distort measurement. But the error put aside, one can note that, in a general way, a dating with carbon-14 is never reliable at 100%. The inaccuracy is sometimes tiny (approximately 5% for the most precise), but, being given the important age of the samples, this error can sometimes represent more than nine centuries. From where the prudence with which it is sometimes necessary to interpret this kind of results.
This method is based on the calculation of 14C/12C proportion. It was considered a long time that disintegration was done in a uniform and regular way. However, for a few years already, the scientists have realized that this disintegration was not inevitably regular. It was thus necessary to recalibrate the tables which match up the proportion of carbon-14 still present in the sample and the age of this one.
One also could note through the dating of several objects that the natural variation of the magnetic field of the Earth can, although being extremely tiny, influence the disintegration of the carbon-14 atoms in carbon 12 atoms (just like the temperature can also play a part). Other assumptions exist. The presence of micro-mushrooms in the fabric could « have renovated it » thus distorting the measure made by the mass spectrometer. But only a thorough study would make it possible to validate this idea.
What can be the causes
of the errors of dating ?
The various fires which the Shroud had to undergo during centuries could very well "reload" the fabric in carbon-14, distorting by the same occasion the measurements taken later on. This phenomenon took, these fifty last years, a considerable importance due to the human activity. Pollution and more particularly the rejection in the atmosphere of huge quantities of carbon dioxide distorted in a very significant way the measurements carried out on more contemporary objects.
In the same way, the many atmospheric nuclear tests carried out in the Fifties and Sixties as well as the incidents of the civil nuclear power (Tchernobyl, Harrisburg...) made considerably vary the proportion of 14C/12C (it is estimated that the tests on the bomb H carried out into 1962 resulted in to double in one year the content of 14C of the Earth's atmosphere). Even the measuring instruments can be disturbed in certain cases by the ambient radioactivity, making then measurements hazardous. This phenomenon could be emphasized by the low size of the sample provided to the scientific team, because of the symbolic value that this fabric has for the Christians.
DATING OF OTHER RELICS
The dating method applied to other relics
Another object was thus prone to debate: it is the Chair of St Peter in the Vatican. According to the tradition it would be the « episcopal throne of the apostle Peter », (thus called since 1230), but this was rejected. The wood of this Chair has also dated from the Middle Ages. In fact, this Chair, the saint's supposed throne now encased in a Bernini reliquary, is made of several woods variously dated back to 4th-6th and 10th -12th centuries AD. It is probably the work of pagan craftsmen and undoubtedly was reconverted later in lithurgic use.
A fragment of the True Cross, now in the Stavelot Triptych in the Pierpont Morgan collection, New York, is dated to AD. 595±115. (Calvin's gibe that there were enough fragments of the True Cross to build 'a good ship' is unfair. An 1870 calculation estimates the volume of the Cross at 178 million cubic millimetres, of which only 4 million survive in relics; a satisfactory 174 million have succumbed to taphonomic processes.) With the Pierpont Morgan fragment is a piece of the Virgin's robe, carbon-dated to the 13th century AD.
No shroud has been carbon-dated before. The standing of the Cadouin shroud in France, the leading previous pretender, has not recovered since 1934, when it was found to have been woven in Egypt during the 10th century AD; its decorative embroidered bands bless Allah in Kufic script. There are also rival tunics of the Passion in Argenteuil and Trier, as well as an another shroud in Besançon. The scientific tests on the Argenteuil tunic, made before its abduction by the french terrorist group Action Directe in 1983 (the first relic to be held to terrorist ransom), are said to show it was woven at about the time of Christ.
In conclusion
One can say to conclude that the method of dating by the carbon-14 cannot in any case to be regarded as a single means to date an object. As we saw in this small study it is essential, on the one hand, to correlate the results obtained by the C14 with the known history of the object, and, on the other hand, to try to match up these results with those which the dendrochronology, the thermoluminescence, or the electromagnetism influence on the measurement could give.
All these subjects are also dealt
in the CDs available on this website :
(1) The Mandylion: a 2000-year-old enigma,
François Gazay, Mersi Multimedia, 2000
(2) Order of Templars:
the strange worship of the magic head,
François Gazay, Mersi Multimedia, 2005
(3) The controversy of Turin: true Relic or forged Shroud ?,
François Gazay, Mersi Multimedia, 2006
To have a brief survey and to get these CDs, click HERE.